Concept cartoons: fysiska och kemiska förändringar, årskurs 7-9
Här hittar du concept cartoons om fysiska och kemiska förändringar. Med serieteckningar får du igång elevernas diskussioner om naturvetenskapliga frågor, till exempel: När kondenserar vattenånga?
Stöd och inspiration till undervisning i fysik och kemi för årskurs 7–9. Med concept cartoons om fysiska och kemiska förändringar kan eleverna utbyta idéer och fördjupa sig i frågeställningarna. Till varje concept cartoon finns idéer till arbete med eleverna och en naturvetenskaplig förklaring.
Se kopplingen till grundskolans läroplan och det centrala innehållet i kursplanerna för fysik och kemi:
Grundskolans läroplan och kursplaner
Här hittar du vårt samlade stödmaterial med concept cartoons inom naturvetenskap:
Vattenånga
Fysik och kemi årskurs 7–9.

När blir det vattenånga av vattnet?
A. Sätt torktumlaren på högsta temperaturen. Vatten förångas inte om temperaturen är mindre än 100 ° C.
B. Vattnet förångas snabbare vid högre temperaturer.
C. Vatten förångas vid exakt 100 ° C.
D. Vattnet avdunstar vid alla temperaturer.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: När blir det vattenånga av vattnet Pdf, 394 kB, öppnas i nytt fönster.
Pdf, 394 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan planera och genomföra en undersökning där de jämför hur fort vatten avdunstar vid olika temperaturer. De kan hälla lika mycket vatten i tre likadana kärl och ställa dem på samma ställe. Vattnet i de olika kärlen ska då ha olika temperatur. Sedan jämför de hur vattennivån ändras. De gör då en systematisk undersökning – en fair test. De kan sedan diskutera olika sätt att torka kläder.
Naturvetenskapligt innehåll
När en vätska blir varmare rör sig partiklarna snabbare. De rör sig i alla riktningar. När partiklarna kolliderar med varandra överförs energi mellan dem och de rör sig snabbare och längre sträckor. När vatten värms upp i torktumlaren rör sig alltså molekylerna snabbare och vattnet övergår till gasform. Ju varmare desto fortare går det. Även i rumstemperatur avdunstar vattnet. Det beror på att en del molekyler får tillräckligt med energi för att lämna vätskan.
Våt tvätt torkar fortare i torr luft och om det blåser. Luft kan bara hålla en viss mängd vattenånga vid en viss temperatur. Stiger fuktigheten kondenserar ångan. Om det är mycket stilla runt tvätt som torkar kan luften närmast tyget bli mättat med vattenånga. Om det blåser åker molekylerna iväg och det torkar fortare.
Kondensation
Fysik och kemi årskurs 7–9.

När kondenserar vattenånga?
A. Kondensation beror på hur mycket vatten det finns i luften, inte på temperaturen.
B. Vattenånga kondenserar och det blir imma på fönstret när det är kallt ute.
C. Ibland avdunstar snö direkt utan att bli vatten.
D. Ibland kan ånga bli is utan att de bildas vatten.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: När kondenserar vattenånga Pdf, 712 kB, öppnas i nytt fönster.
Pdf, 712 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan börja med att berätta om var och när de kan se kondens – imma och dimma. De kan också diskutera vilka omständigheter som då råder. Ett sätt att visa kondens är att ta en flaska ur ett kylskåp och ställa den i rumstemperatur. Eleverna kan diskutera kondens, regn och snö.
Naturvetenskapligt innehåll
Kondensation är en process där gas omvandlas till vätska. När vattenånga träffar en kall yta omvandlas den till den vatten i flytande form och det bildas små droppar på den kalla ytan. Det kallas kondens. Det sker på vindrutor på vintern eftersom glaset är kallt. Det kan också ske vid högre temperaturer om luften innehåller mycket vattenånga. Om man rör sig på platser där det är mycket varmt och fuktigt kan vattenångan i luften bilda kondens i kontakt med exempel huden.
Ibland avdunstar snö utan att det bildas vatten, istället går snön direkt över till vattenånga. Det kallas sublimering. Om temperaturen är under 0 ° C kan vattenångan omvandlas direkt till is utan att vätska bildas. Man ser det ibland som istappar. Det kallas desublimering.
Sockerlösning
Fysik och kemi årskurs 7–9.

Vad händer när socker löses?
A. Häll inte för mycket te i min kopp, det måste finnas plats för socker.
B. Volymen ändras nästan inte alls när du lägger i socker.
C. Den totala volymen är volymen av teet plus volymen av socker.
D. Volymen ökar först, men minskar när sockret löses upp.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: Vad händer när socker löses Pdf, 474 kB, öppnas i nytt fönster.
Pdf, 474 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan planera och genomföra en undersökning där de tar reda på hur massa och volym ändras när de löser socker i varm vätska. De kan också undersöka hur mycket socker de kan lösa i en viss volym. Eleverna kan diskutera vardagliga exempel som syltkokning.
Naturvetenskapligt innehåll
När socker löses i vatten blandas sockermolekyler med vattenmolekylerna och man ser inte längre sockret. Sockermolekylerna rör sig i utrymmena mellan vattenmolekylerna och volymen ändras i princip inte. Det vita sockret löses och syns därför inte. Men sockret har inte försvunnit och det känner man om man smakar på vätskan. Om man tillsätter otillräckligt mycket socker blir vätskan mättad och sockret faller ut. I en varm vätska kan lösa mer socker lösas än i en kall. Om vätskan får avdunsta faller sockret ut.
Neutralisation
Kemi årskurs 7–9.
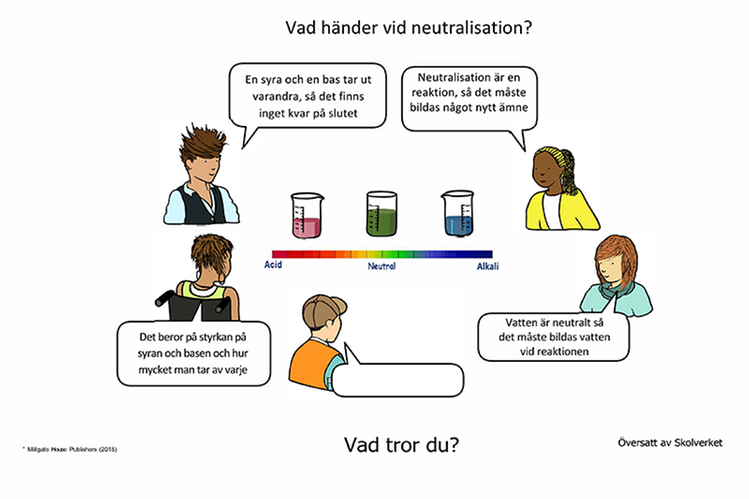
Vad händer vid neutralisation?
A. En syra och en bas tar ut varandra, så det finns inget kvar på slutet.
B. Neutralisation är en reaktion, så det måste bildas något nytt ämne.
C. Vatten är neutralt så det måste bildas vatten vid reaktionen.
D. Det beror på styrkan på syran och basen och hur mycket man tar av varje.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: Vad händer vid neutralisation Pdf, 524 kB, öppnas i nytt fönster.
Pdf, 524 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan diskutera vad surt och basiskt är och hur man mäter detta. De kan ge förslag på sura och basiska ämnen och mäta pH i vatten och i lösningar med några av de föreslagna ämnena. Eleverna kan använda universalindikatorpapper eller pH-meter. De kan fortsätta med att neutralisera syror och baser och mäta pH. Sedan kan de diskutera pH i olika sammanhang, till exempel i organen i matspjälkningsapparaten och i olika jordar, och vad det betyder.
Naturvetenskapligt innehåll
pH-skalan är logaritmisk och pH anger halten av vätejoner (oxoniumjoner). I en vattenlösning finns nämligen vätejonerna i form av oxoniumjoner (H3O+). Hydroxidjoner betecknas OH-. Om en vätska innehåller fler vätejoner än hydroxidjoner är dess pH-värde lägre än 7. Om en vätska innehåller lika många vätejoner och hydroxidjoner är dess pH-värde lika med 7. Om en vätska innehåller färre vätejoner än hydroxidjoner är dess pH-värde högre än 7.
Neutralisation är en reaktion mellan en syra och en bas. Den kan skrivas som: syra + bas → salt + vatten. Exempel: saltsyra + natriumhydroxid → natriumklorid + vatten. Ett salt är en förening som består av en metalljon och en icke-metalljon.
Rost
Kemi årskurs 7–9.

Vad orsakar rost?
A. Cyklar tillverkas inte av järn längre eftersom järn tar upp rost från andra rostiga saker.
B. När järn blir rostigt, ändras inte järnet, det får bara en annan färg.
C. Järn kan inte smittas av rost. Rost är järn som förvandlats till en kemisk förening.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: Vad orsakar rost Pdf, 689 kB, öppnas i nytt fönster.
Pdf, 689 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan diskutera och ta reda på skillnaden mellan grundämne, kemisk förening och blandning. De kan fundera på under vilka omständigheter det rostar och hur det ser ut och även studera rostiga föremål till exempel spik. De kan jämföra egenskaperna hos en rostig spik med en som inte rostat, ta reda på vad rost är och vilken kemisk beteckning det har. Sedan kan de diskutera vilka problem det innebär när det rostar i olika sammanhang och hur detta kan förhindras.
Naturvetenskapligt innehåll
Rostning är en kemisk reaktion som sker när järn reagerar med syre från luften och bildar järnoxid. Tvåvärt järn finns i den röda rosten. Oxidationen kan sedan fortsätta och en mörkare rost med trevärt järn bildas. I fuktig luft reagerar järnoxiderna med vatten till järnhydroxid. Rost är alltså en blandning av järnoxider och järnhydroxid.
Det rostar mer i fuktig luft. Det är en ganska långsam kemisk reaktion, så det är svårt att se att det hända. Man får studera objekt med vissa tidsintervall under en längre tid. Rostigt järn tar större plats än järn vilket gör att rosten, beroende på var den bildads, kan få sprängkraft och förstöra järnkonstruktioner. Järn och syre är grundämnen och järnoxid är en kemisk förening.
Brinnande magnesium
Kemi årskurs 7–9.

Magnesium brinner
A. När magnesium brinner blir det aska och biten blir lättare.
B. Det blir tyngre eftersom partiklarna reagerar med syre i luften.
C. Vikten blir samma eftersom partiklarna inte har förändrats.
D. Det blir lättare eftersom rök försvinner i luften.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: Magnesium brinner Pdf, 602 kB, öppnas i nytt fönster.
Pdf, 602 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Det kan vara bra att göra en demonstration med magnesium som brinner och diskutera olika möjligheter med eleverna. Eleverna kan väga en tuss stålull, bränna den på ett säkert sätt och väga den igen. De kan jämföra sina resultat och förklara varför det blir så. De kan sedan diskutera likheter och skillnader mellan experimenten med magnesium och järn.
Naturvetenskapligt innehåll
När magnesium brinner reagerar det med syre i luften och det bildas ett nytt ämne – magnesiumoxid. Alla magnesiumatomer finns kvar men har förenats med syre till molekyler och resultatet blir att massan ökar. Samma sak gäller för järn som brinner. Också här sker en kemisk reaktion med luftens syre. Metaller som till exempel natrium och kalium är reaktiva och bildar oxider utan att behöva brännas. Det räcker med luftens syre för att reaktionen ska komma i gång. Därför förvaras sådana metaller till exempel i fotogen.
Kemiska reaktionsformler
Kemi årskurs 7–9.

Vad betyder siffrorna i kemiska reaktionsformler?
A. Siffrorna betyder att du behöver två mått av magnesium och två puffar av syret.
B. Talen i reaktionsformeln går inte jämt ut. Två tvåor på vänstra sidan gör att det borde stå fyra på den högra sidan.
C. Siffrorna visar hur många atomer av varje slag som reagerar med varandra.
D. Siffrorna betyder att du behöver två gram magnesium och två gram syre.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Idéer för arbete med eleverna
Eleverna ka få några exempel på reaktionsformler och diskutera vad siffrorna står för. Med hjälp av periodiska systemet kan de beskriva vilka reaktioner som är möjliga och förklara de olika föreningarnas uppbyggnad. De kan använda molekylmodeller för att illustrera och testa olika kombinationer.
Naturvetenskapligt innehåll
I periodiska systemet finns alla grundämnen. De är uppbyggda av atomer. Gruppnumret anger antalet elektroner i det yttersta elektronskalet. Beroende på antalet elektroner i det yttre elektronskalet kan grundämnen reagera med varandra på olika sätt och bilda kemiska föreningar.
Den kemiska formeln anger antalet av varje atomslag i en molekyl. I en kemisk reaktion kombineras atomerna om. Inga atomer kommer till och inga försvinner. Därför är antalet atomer av varje slag lika före och efter att den kemiska reaktionen skett. När man skriver en reaktionsformel måste den därför balanseras så att det blir lika många av varje atomslag på båda sidor.
Kemiska reaktioner
Kemi årskurs 7–9.

Hur ändras temperaturen vid kemiska reaktioner?
A. Vid kemiska reaktioner blir det varmt.
B. Vid vissa kemiska reaktioner förändras inte temperaturen.
C. Vid vissa kemiska reaktioner blir det kallt.
D. Det måste tillföras värme för att reaktionen ska komma igång.
Vad tror DU?
Ladda ner och skriv ut bilden i större format:
Concept cartoon: Hur ändras temperaturen vid kemiska reaktioner Pdf, 696 kB, öppnas i nytt fönster.
Pdf, 696 kB, öppnas i nytt fönster.
Idéer för arbete med eleverna
Eleverna kan berätta om några reaktioner där det blir varmt. Sedan kan de göra ett experiment där de mäter temperaturen i en bägare med vinäger, sätter till bakpulver och mäter igen. De kan få bekanta sig med begreppen endoterm och exoterm och applicera begreppen på några olika reaktioner.
Naturvetenskapligt innehåll
Kemiska reaktioner innebär att energi omvandlas. I organiska ämnen är kemisk energi bunden. När det brinner reagerar det organiska ämnet med syre och det bildas koldioxid och vatten. Samtidigt omvandlas den kemiska energin till bland annat värmeenergi och temperaturen stiger. Det är en exoterm reaktion. Andra reaktioner är endoterma. Då absorberas värme och binds in som kemisk energi. Så är fallet då ättiksyra (vinäger) reagerar med natriumvätekarbonat (bakpulver).
Vissa reaktioner kräver hög temperatur för att komma igång, men fortsätter sedan själva, som till exempel då magnesium bränns. Vissa reaktioner innebär inte någon märkbar temperaturförändring.